8.3. Принципы стабилизации полимеров в целях защиты их от старения
Старение полимеров представляет сумму физико-химических изменений их исходной структуры, под воздействием химических реакций, протекающих под действием тепла, света, радиационных излучений, механических напряжений, кислорода, озона, кислот, щелочей. Эти реакции приводят к деструкции полимерных цепей или их нежелательному, неконтролируемому сшиванию, в результате чего полимеры становятся липкими и мягкими (деструкция) или хрупкими и жесткими (сшивание), а главное - менее прочными. В реальных условиях эксплуатации полимерных изделий на них действует одновременно несколько из перечисленных факторов. Например, солнечный свет, кислород воздуха, озон. Для стран с жарким климатом на это накладывается еще повышенная температура, влажность. При работе многие полимерные изделия разогреваются (например, при многократных деформациях эластомеров) или используются для работы в условиях повышенных температур, в результате чего интенсивно развиваются термическое и термоокислительное старение полимеров.
Таким образом, проблема защиты полимеров от старения является комплексной и должна учитывать все эти факторы. Уже из краткого рассмотрения видов деструктирующих воздействий на полимеры можно заключить, что главными из них являются термическая и термоокислительная деструкции, усиливающиеся при одновременном действии света. Эти процессы протекают главным образом по механизму цепных радикальных реакций. Следовательно, меры защиты должны быть в первую очередь направлены на подавление этих реакций в полимерах. Из рассмотрения химических свойств и реакций полимеров мы знаем, что благодаря высокомолекулярной природе полимеров очень малые количества низкомолекулярных химических реагентов способны вызывать существенные изменения физических и механических свойств полимеров. Это в полной мере относится и к кислороду как наиболее распространенному химическому агенту, в контакте с которым работают полимерные изделия. Следовательно, для защиты полимеров от этих вредных воздействий или для стабилизации полимеров и изделий из них во времени можно использовать малые добавки низкомолекулярных веществ, которые будут прерывать развитие цепных реакций, например окисления. Такие вещества, как мы знаем, называются ингибиторами
цепных реакций. Следовательно, проблема стабилизации полимеров - это главным образом проблема поиска эффективных ингибиторов, или стабилизаторов, которые, будучи добавлены в полимер в очень малых количествах, не давали бы возможности развиваться нежелательному цепному процессу деструкции макромолекул.
Рассмотрим основные пути стабилизации полимеров и определим круг веществ, которые выполняют функцию стабилизаторов. Поскольку стабилизация связана, главным образом, с защитой полимера от действия кислорода, тепловых и световых воздействий, то эти стабилизаторы часто называют
противостарителями; они служат и как антиоксиданты, т. е. вещества, препятствующие развитию цепи окислительных реакций в полимерах.
По механизму действия антиоксиданты делятся на две большие группы. К первой относятся вещества, обрывающие окислительную цепь реакций, т. е. ингибиторы, реагирующие со свободными радикалами на стадии их образования. Сюда относятся широко применяемые в практике антиоксиданты аминного и фенольного типа. Ко второй группе относятся вещества, предотвращающие разложение гидроперекисей по радикальному механизму, т. е. разрушающие гидроперекиси до неактивных для развития окислительной цепи продуктов. Это так называемые антиоксиданты превентивного действия, к которым относятся сульфиды, меркаптаны, тиофосфаты, соли диалкилдитиокарбаминовых кислот. Антиоксиданты первой группы характеризуются наличием в их молекуле подвижного атома, который отрывается и участвует в радикальных реакциях легче, чем активные атомы водорода молекул полимера. Образующиеся при этом свободные радикалы ингибитора малоактивны и не могут вызвать продолжение цепи радикальных реакций. Если обозначить молекулу ингибитора InH, то схема реакции обрыва окислительной цепи выглядит так:
InH + ROO· -> ROOH + In· In· + In· -> In—In неакт. молекула
InH + RO· -> ROH + In·
Ингибиторы этого типа увеличивают длину индукционного периода окисления на кинетической кривой. После исчерпания ингибитора процесс окисления продолжается (рис.74).
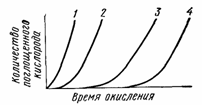
Рис. 74. Кинетические кривые окисления полипропилена при 140° С в присутствии различных антиоксидантов в эквимолярных количествах:
1 — без антиоксиданта; 2 — бензидин;
3 — дифениламин; 4 — фенил-b-нафтиламин
Защитное действие антиоксидантов, которое характеризуется величиной индукционного периода на кривой поглощения кислорода при данной температуре, зависит от количества примененного антиоксиданта. Существует критическая концентрация его в полимере, ниже которой защитное действие не проявляется, и оптимальная концентрация, при которой индукционный период имеет наибольшую длину. Ниже и выше оптимальной концентрации величина индукционного периода заметно снижается (рис.75).
Антиоксиданты превентивного действия, например, тиофосфаты, обычно не влияют на величину индукционного периода, но сильно снижают скорость присоединения кислорода к полимеру в главном периоде процесса. Чрезвычайно важным в практическом отношении является синергизм, т. е. взаимоусиление действия смеси двух антиоксидантов первой и второй групп. Если применить два слабых антиоксиданта из этих групп раздельно, то величина индукционного периода будет невелика.
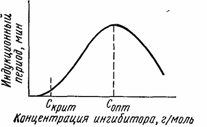
Рис. 75. Зависимость величины индукционного периода окисления полимеров от концентрации ингибитора окисления (указаны критическая и оптимальная концентрации ингибитора)
Если же применить их смесь, общая концентрация которой в полимере будет постоянна, то наблюдается увеличение индукционного периода по сравнению с аддитивной величиной, которое имеет резкий максимум при близких молярных концентрациях этих антиоксидантов (рис.76).
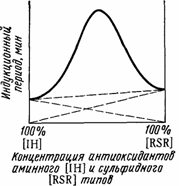
Рис. 76. Синергизм защитного действия при совместном применении в качестве антиоксидантов в полимерах аминов и сульфидов
Таким действием обладает, например, смесь дилаурилтиодипропионата (антиоксидант превентивного действия) и ионола (антиоксидант, обрывающий окислительную цепь) для стабилизации полипропилена или фосфата и фенола для ненасыщенных полимеров.
Рассмотрим более подробно действие антиоксидантов при окислении полимеров. Фенолы и ароматические амины содержат в своих молекулах слабо связанный атом водорода, который обрывает цепи окисления. Однако водород в молекуле антиоксиданта InH может при больших его концентрациях реагировать не только со свободными радикалами окислительной
цепи, но и с молекулярным кислородом:
InH + О2 -> In· + HО2·
Этим объясняется уменьшение величины индукционного периода после оптимальной концентрации ингибитора (см. рис. 75). Радикал НО2· реагирует с полимером (RH) с развитием цепи окисления:
HО2· + RH -> R· + H2О2
Кроме того, образующаяся при обрыве цепи антиоксидантом молекула гидроперекиси полимера (RО2 + InH -> ROOH + In·) может распадаться с образованием двух активных радикалов (ROOH -> RO·+ОH·), что приведет к вырожденному разветвлению цепи.
Радикалы ингибитора мало активны и реагируют либо друг с другом, либо с другими радикалами, обрывая, таким образом, реакционные цепи:
Iп· + In· -> In—In; In· + RO2 -> ROOln
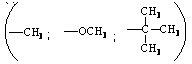 Фенольные антиоксиданты обычно содержат в молекуле фенола различные заместители в орто - и параположениях. Увеличение активности антиоксиданта достигается введением электронодонорных заместителей:
Фенольные антиоксиданты обычно содержат в молекуле фенола различные заместители в орто - и параположениях. Увеличение активности антиоксиданта достигается введением электронодонорных заместителей:
Увеличению активности способствует также введение разветвленных алкильных заместителей только в орто-положение. Примером такого типа антиоксиданта является ионол (4-метил-2,6-дитретбутилфенол:
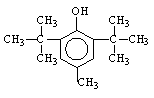
Или бис-фенол-2,2-метилен-бис (4-метил-6-третбутилфенол):
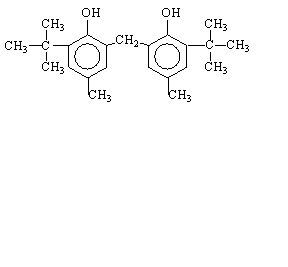
(антиоксидант 2246)
Широко распространены антиоксиданты типа вторичных ароматических аминов, действующие аналогично фенолам (содержат подвижный атом водорода). Обычно амины активнее фенолов. Например, фенил-b-нафтиламин (неозон D) действует по схеме
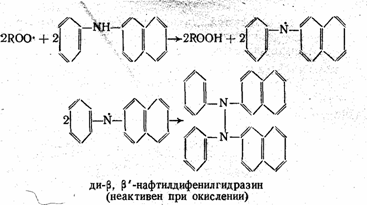
Введение гидроксила или метоксигруппы в пара-положение фенольного заместителя при атоме азота увеличивает эффективность защитного действия антиоксиданта. Еще более активны производные, содержащие две аминогруппы: N-фенил-N¢-изопропил-парафенилендиамин (антиоксидант 4010 NA)
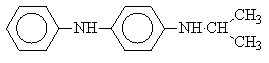
и N, N¢-дифенил-пара-фенилендиамин (нонокс):
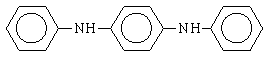
Все указанные антиоксиданты при концентрациях менее 1-2% эффективно защищают полимеры.
Превентивные антиоксиданты в отличие от фенольных и аминных разлагают перекиси и гидроперекиси, образующиеся на начальных этапах окисления полимеров, до неактивных продуктов. Присутствие этих антиоксидантов особенно важно, если в полимере содержатся соли металлов переменной валентности — активные катализаторы окисления:
ROOH + Cu2+ -> RO2· + Cu+ + H+ ü
ý 2ROOH ->RO2·+RO·+H2O
ROOH + Cu+ -> RO· + Cu2+ + OH-þ
Превентивный антиоксидант диэтилдитиокарбамат цинка
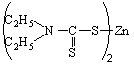
образует комплекс с этим металлом, который не ионизован и таким образом не может влиять на развитие окислительной цепи:
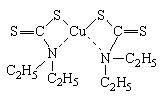
Гидроперекиси разлагаются дитиокарбаматами, дитиофосфатами, сульфидами, меркаптанами. Например, органические сульфиды разлагают гидроперекиси по схеме:
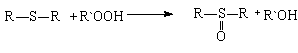
Вероятно, синергизм действия смеси амина и сульфида объясняется тем, что первый компонент при обрыве цепи окисления дает молекулу гидроперекиси (см. выше), а второй разрушает ее, увеличивая время жизни первого компонента (амина), поскольку уменьшается число окислительных цепей. Амины и фенолы более эффективны при низких температурах окисления, а превентивные антиоксиданты — при высоких.
Кроме этих классов антиоксидантов, эффективную защиту полимеров от окисления оказывают соединения с системами сопряжения, где электроны делокализованы и свободно перемещаются по всей молекуле (как в металлах), и некоторые соединения типа стабильных радикалов. К последним относятся азот-окисные радикалы ароматических и алифатических соединений. Например,
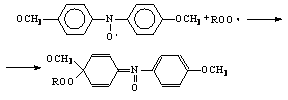
Азот-окисные радикалы, следовательно, обрывают окислительную цепь реакций, дезактивируя радикалы ROO· или R·. Их применение рационально для полимеров, которые не содержат подвижных атомов водорода в макромолекулах (полиформальдегид, полиамид), так как в противном случае азот-окисные радикалы могут отрывать подвижный атом водорода полимера и инициировать цепной процесс окисления.
В настоящее время накоплен большой материал по механизму старения и стабилизации полимеров. Этому способствовало применение ряда современных методов исследования, например, метода электронного парамагнитного резонанса, позволяющего идентифицировать количество и структуру свободных радикалов, образующихся при окислении, термическом, фотохимическом, радиационном, механическом распаде полимеров, метода ядерного магнитного резонанса и др. Большой вклад в развитие наших знаний о старении и стабилизации полимеров внесли труды советских ученых— Н. Н. Семенова, Н. М. Эмануэля, А. Н. Баха, М. Б Неймана и др. Широко проведенные исследования позволили разработать эффективные методы стабилизации различных классов полимеров. Для многих из них разработаны меры комплексной защиты от теплового, термоокислительного, светоозонного, радиационного старения. При этом оценка эффективности противостарителей осуществляется не только по активности в химических реакциях, но и по растворимости в полимере, летучести, термостабильности и другим факторам. Полиэтилен, например, хорошо защищается от термоокислительной деструкции в присутствии небольших количеств (0,01%) фенольных или аминных антиоксидантов, что важно для его переработки. При эксплуатации полиэтилен достаточно стабилен, тогда как полипропилен нуждается в антиоксидантах для защиты от старения при эксплуатации. Здесь более эффективны производные фенилендиаминов. Для защиты полиэтиленовых пленок от действия ультрафиолетового света применяют бис-фенолы. Весьма важна проблема стабилизации ненасыщенных полимеров (каучуков), где достаточно эффективны аминные противостарители или их сочетание с превентивными антиоксидантами.
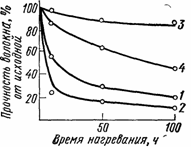
Рис. 77. Изменение прочности полиамидного волокна (капрон) в зависимости от времени нагревания при 150 (1, 3) и 180° С (2, 4) (стабилизатор N, N¢-ди-b-нафтил-пара-фенилендиамин введен в процессе полимеризации) • 1, 2 - без стабилизатора, 3, 4 - со стабилизатором
При стабилизации поливинилхлорида надо учитывать, что он отщепляет хлористый водород уже при обычных условиях эксплуатации. Этот процесс ускоряется под действием солнечного света, нагревания и сопровождается появлением хрупкости и изменением цвета у изделий из поливинилхлорида. Переработка поливинилхлорида проводится при температурах 170-190°С, что требует присутствия термостабилизаторов. Процесс термодеструкции осложняется еще и окислительными реакциями. Поэтому в качестве стабилизаторов в этом случае используют смеси различных веществ (5-6 компонентов): стеараты свинца или кадмия, основные соединения (для поглощения НС1), бензофенолы (защитаотультрафиолетовых лучей), фосфиты (разложение перекисей).
Кроме того, могут вводиться еще вещества, связывающие продукты реакции указанных типов стабилизаторов с НС1 и другими веществами.
Освещение полиамидных пленок приводит к увеличению их оптической плотности (по сравнению с хранением в темноте).
При освещении полиамидов образуются свободные радикалы:

и т. д.
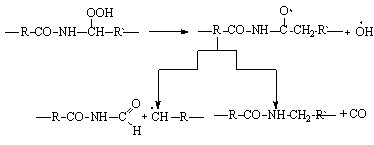
Гидроперекиси распадаются далее, приводя к деструкции макромолекул:
Окись углерода была обнаружена в продуктах деструкции. Старение полиамидов под действием солнечного света является одной из сложных проблем стабилизации этого класса полимеров.
Проблема стабилизации полимеров является весьма сложной и многоплановой, так как здесь приходиться учитывать влияние не только различных факторов старения, но и химическую и физическую структуру полимеров. Поэтому детальное изучение процессов старения проводится обычно для каждого класса полимеров отдельно.











