5.6. Мембранные процессы
Частицы растворенного вещества и растворителя находятся в беспорядочном тепловом движении и равномерно распределяются по всему объему раствора. Если поместить в емкость концентрированный раствор какого-либо вещества, а поверх него осторожно налить слой более разбавленного (менее концентрированного) раствора, то через некоторое время молекулы растворителя и растворенного вещества равномерно распределятся по всему объему жидкости. Самопроизвольный процесс перемещения молекул вещества, приводящий к выравниванию концентраций в растворе, называется диффузией. Диффузия, при которой процесс проникновения молекул в результате беспорядочного теплового движения осуществляется в обоих направлениях: из раствора с высокой концентрацией в раствор со слабой концентрацией, и наоборот, из раствора со слабой концентрацией в раствор с высокой концентрацией – называется встречной или двусторонней.
Осмосом называется односторонняя диффузия через полупроницаемую перегородку – мембрану. Осмотическое давление раствора – количественная характеристика осмоса – равно гидростатическому давлению, при котором достигается (наступает) равновесие при односторонней диффузии через полупроницаемую мембрану. Полупроницаемая мембрана – это такая мембрана, через которую растворитель может проходить, а растворенное вещество нет. Такие перегородки существуют в природе, а также могут быть получены искусственно.
При измерениях осмотического давления различных растворов было установлено, что величина осмотического давления зависит от концентрации раствора и от его температуры, но не зависит ни от природы растворенного вещества и ни от природы растворителя.
Закон Вант-Гофа показывает для растворов электролитов невысоких концентраций зависимость осмотического давления от концентрации и температуры раствора
P = C·R·T, (1.25)
где Р – осмотическое давление раствора, кПа; С – объемная мольная концентрация раствора (молярность), моль/л; R = 8,314 Дж/моль – универсальная газовая постоянная; Т – абсолютная температура раствора, К.
Молярность раствора представляет собой отношение количества растворенного вещества к объему V в литрах
C= n/ V. или C = m / (M – V). (1.26)
Подставляя выражение (1.26) в (1.25), получим:
P.V= m·R·T / M. (1.27)
Это уравнение позволяет по величине осмотического давления раствора определять мольную массу, а значит, и молекулярную массу растворенного вещества, следовательно, и объем выделяемого из раствора вещества.
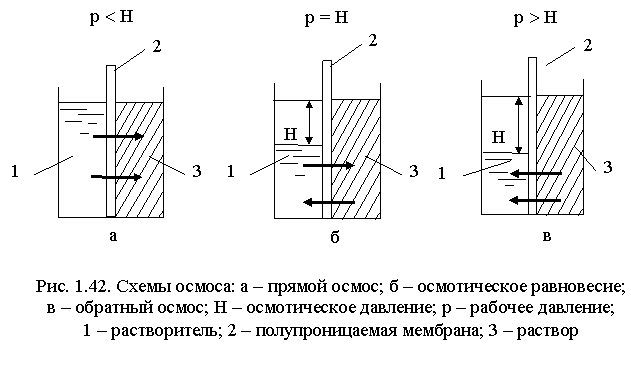
Если к раствору, отделенному от растворителя полупропорциональной мембраной, приложить внешнее давление (рис. 1.41), равное осмотическому давлению раствора, то осмос прекратится, следовательно, установится осмотическое равновесие.
Если же приложенное внешнее давление превысит осмотическое, то диффузия растворителя будет преимущественно происходить из раствора в фазу растворителя, т.е. в направлении, противоположном направлению переноса растворителя при осмосе. Такое явление получило название обратного осмоса. Таким образом, это непрерывный процесс молекулярного разделения растворов путем их фильтрования под давлением через полупроницаемые мембраны, задерживающие полностью или частично молекулы, или ионы растворенного вещества.
Осмос широко применяется как один из наиболее экономичных способов опреснения воды. Солевой раствор (например, морская вода) отделяют полупроницаемой мембраной от пресной воды и подвергают давлению, более высокому, чем осмотическое давление раствора. В результате часть содержащейся в растворе воды "вытесняется" в пресную воду, а концентрация соли в оставшемся растворе повышается. Концентрированный солевой раствор периодически заменяется свежими порциями морской воды, подлежащей опреснению. Обратный осмос также используется для обессоливания воды в системах водоподготовки ТЭЦ и предприятий различных отраслей промышленности (полупроводников, кинескопов, медикаментов и др.); в последние годы начинает применяться для очистки некоторых промышленных и городских сточных вод. В процессе ультрафильтрации получают концентрат, содержащий органические вещества, а в процессе обратного осмоса – концентрат неорганических веществ и чистую воду.
Обратным осмосом и ультрафильтрацией называются процессы фильтрования растворов через полупроницаемые мембраны под давлением, превышающим осмотическое давление.
Мембраны пропускают молекулы растворителя, задерживая растворенные вещества. При обратном осмосе отделяются частицы (молекулы, гидратированные ионы), размеры которых не превышают размеров растворителя. При ультрофильтровании размер отдельных частиц dч на порядок больше. Условные границы применения этих процессов приведены в табл. 1.4.
Таблица 1.4
| Процесс | dч, mkm |
| Обратный осмос | 0,0001 0,001 |
| Ультрафильтрация | 0,001-0,02 |
| Макрофильтрация (гиперфильтрация) | 0,02-10 |
Таким образом, от обычной фильтрации такие процессы отличаются отделением частиц меньших размеров. Давление, необходимое для проведения процесса обратного осмоса (6-10 МПа), значительно больше, чем для процесса ультрафильтрации (0,1-0,5 МПа).
Достоинства метода:
- Отсутствие фазовых переходов при отделении примесей, что позволяет вести процесс при небольшом расходе энергии.
- Возможность поведения процессов при комнатных температурах без применения или с небольшими добавками химических реагентов.
- Простота конструкции аппаратуры.
Недостатки:
- Возникновение явления концентрационной поляризации, которое заключается в росте концентрации растворенного вещества у поверхности мембраны. Это приводит к уменьшению производительности установки, степени разделения компонентов и срока службы мембран.
- Проведение процесса при повышенных давлениях, что вызывает необходимость применения специальных уплотнений для аппаратуры.
Эффективность процесса зависит от свойств применяемых мембран. Они должны обладать следующими достоинствами:
- высокой разделяющей способностью (селективностью);
- большой удельной производительностью (проницаемостью);
- устойчивостью к действию среды;
- постоянством характеристик в процессе эксплуатации;
- достаточной механической прочностью;
- низкой стоимостью.
Селективность процесса разделения определяют по формуле

где С0 – концентрация растворенного вещества в исходной воде; Сф – концентрация растворенного вещества в фильтрате.
Проницаемость определяется количеством фильтрата, получаемого в единицу времени с единицы рабочей поверхности
![]() (1.28)
(1.28)
где Δр – разность давлений воды до и после мембраны; Δр0 – разность осмотических давлений; Кl – коэффициент пропорциональности, зависящий от проницаемости мембран.
Из выражения (1.28) видно, что скорость обратного осмоса прямо пропорциональна эффективному давлению (разности между приложенным давлением и осмотическим). Эффективное давление значительно превосходит осмотическое. Осмотическое давление для растворов некоторых солей с концентрацией 1000 мг/л (табл. 1.5).
Таблица 1.5
| Соль | NaCl | Na2SO4 | MgSO4 | CaCl2 | NHCO3 | MgCl2 |
| Осмотическое
давление, кПа |
79 | 42 | 25 | 58 | 89 | 67 |
В процессе очистки сточных вод некоторое количество растворенного вещества проходит через мембрану вместе с водой. Для мембран с высоким эффектом разделения этот проскок практически не зависит от давления и может быть определен по зависимости (К2 – константа для мембран, зависит от ее конструктивных особенностей)
![]() здесь S – проскок растворенного вещества через 1 м2 мембраны, кг/сут.
здесь S – проскок растворенного вещества через 1 м2 мембраны, кг/сут.
Из данной формулы следует: чем выше концентрация загрязнения в исходной сточной воде, тем выше интенсивность проникновения веществ через мембрану. Существует несколько вариантов обратного осмоса.
По одному из них мембраны собирают воду, которая в поверхностном слое не обладает растворяющей способностью. Если толщина слоя адсорбированных молекул воды составляет половину или более половины диаметра пор мембран, то под давлением через поры будет проходить только чистая вода, несмотря на то, что размер многих ионов меньше, чем размер молекул воды. Прониканию таких ионов через поры препятствует возникающая у них гидратная оболочка. Размер гидратных оболочек различен у разных ионов. Если толщина адсорбированного слоя молекул воды меньше половины диаметра пор, то вместе с водой через мембрану будут проникать и растворенные вещества.
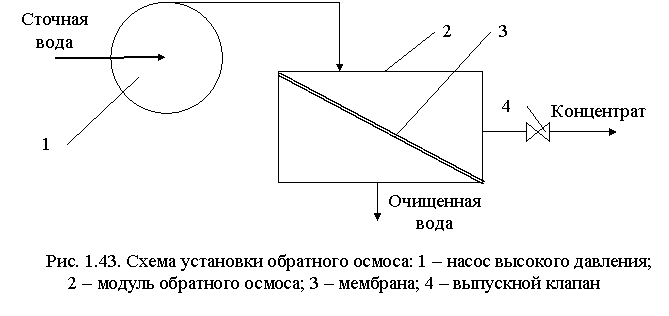
Простейшая установка обратного осмоса (рис. 1.43) состоит из насоса высокого давления и модуля, соединенных последовательно.
Для ультрафильтрации предложен другой механизм разделения. Растворенные вещества задерживаются на мембране потому, что размер их молекул больше, чем размер пор мембраны (табл. 1.4).
В действительности в процессе обратного осмоса и ультрафильтрации имеют место более сложные явления.
Мембранные процессы разделения растворов, осмотическое давление которых мало, называются ультрафильтрацией. Этот метод используется при отделении сравнительно высокомолекулярных веществ, взвешенных частиц, коллоидов. Ультрафильтрация более высокопроизводительный процесс, чем обратный осмос, т.к. проницаемость мембран достигается при давлении 0,2-1,0 МПа.
Очистка сточных вод предприятий целлюлозно-бумажной, химической, нефтехимической и других отраслей промышленности гиперфильтрационными и ультрафильтрационными методами имеет ряд преимуществ перед традиционными методами очистки: невысокие энергозатраты; простота; компактность установок; возможность полной автоматизации; высокая эффективность очистки; возможность повторного использования фильтрата; утилизация полученного концентрата.
Недостатком метода является необходимость проведения процесса при высоком давлении в системе.
Производительность гиперфильтрационных и ультрафильтрационных аппаратов 5-1000 м3/сут. Основным элементом такого аппарата является мембрана, которая прочностью и низкой стоимостью. Схемы работы гиперфильтрационных и ультрафильтрационных аппаратов в зависимости от состава сточных вод, необходимой степени очистки, а также производительности аппаратов могут быть одноступенчатыми и многоступенчатыми.
Для проведения мембранных процессов применяют непористые динамические и диффузионные мембраны, представляющие собой квазимогенные гели, и пористые мембраны в виде тонких пленок, изготовленные из полимерных материалов. Наиболее распространены полимерные мембраны из ацитатцеллюлозы. Разрабатываются мембраны из полиэтилена, фторированного этиленпропиленового сополимера, политетрафторэтилена, пористого стекла, ацитобутирата целлюлозы и др.
Ацетатцеллюлозные мембраны, применяемые для обратного осмоса, имеют анизотропную структуру. Активный верхний слой ее толщиной до 0,25 мкм является слоем, в котором происходит разделение, а нижний – крупнозернистый слой (100-200 мкм) обеспечивает механическую прочность мембран.
Ацетатцеллюлозные мембраны устойчиво работают в интервале давлений 1-8 МПа, температур 0-30 °С и рН = 3-8. Дляультрафильтрации используют нитратцеллюлозные, а также полиэлектролитные мембраны. По структуре они аналогичны ацетатцеллюлозным мембранам.
Процесс мембранного разделения зависит от давления, гидродинамических условий и конструкции аппарата, природы и состава сточных вод, содержания в них примесей, а также от температуры. Увеличение концентрации раствора приводит к росту осмотического давления растворителя, повышению вязкости раствора и росту концентрационной поляризации, т.е. к снижению проницаемости и селективности.
Обратный осмос рекомендуется использовать при следующей концентрации электролитов:
- < 5-10 % – для одновалентных;
- < 10-15 % –двухвалентных;
- < 15-20 % – многовалентных солей.
Для уменьшения концентрационной поляризации организуют рециркуляцию раствора и турбулизацию прилегающего к мембране слоя жидкости, применяя, мешалки, вибрационные устройства и увеличивая скорость.
Природа растворенного вещества оказывает влияние на селективность. При одинаковой молекулярной массе неорганические вещества задерживаются на мембране лучше, чем органические. С повышением давления удельная производительность мембран увеличивается, т.к. растет движущая сила процесса. Однако при высоких давлениях происходит уплотнение материала мембран, что вызывает снижение проницаемости, поэтому для каждого вида мембран устанавливают максимальное рабочее давление.
С ростом температуры уменьшается вязкость и плотность раствора, что способствует росту проницаемости. При этом повышается осмотическое давление, которое уменьшает проницаемость. Кроме того, при повышении температуры начинаются усадка и стягивание пор мембраны, что тоже приводит к уменьшению проницаемости, а также к возрастанию скорости гидролиза и сокращению срока службы мембран. Ацетатцеллюлозные мембраны при температуре 50 0С разрушаются, поэтому необходимо при работе соблюдать рекомендуемый интервал температур. Конструкция аппаратов для проведения мембранных процессов должна обеспечивать большую поверхность мембран в единице объема, простоту сборки и монтажа, механическую прочность и герметичность.
В настоящее время применяются различные типы аппаратов для мембранных процессов, отличающиеся способом размещения и укладки мембраны:
- с плоскокамерными фильтрующими элементами, имеющими удельную площадь поверхности мембран 60-300 м2 на 1 м3 объема аппарата.
- с трубчатыми фильтрующими элементами, имеющие удельную площадь поверхности мембран 60-300 м2 на 1 м3 объема.
- с фильтрующими элементами рулонного или спирального типа с удельной площадью поверхности мембран до 20 000 м2 на 1 м3 объема.
- аппараты с мембранами изготовленными из полых волокон малого диаметра (45-200 мкм), имеющими удельную площадь поверхности до 20 000 м2 на 1 м объема; волокна из ацетатцеллюлозы или нейлона собираются в пучки длиной 2-3 м и располагаются в аппарате линейно или U-образно. Установки обратного осмоса состоят из большого числа элементарных модулей, которые соединяются параллельно или последовательно.
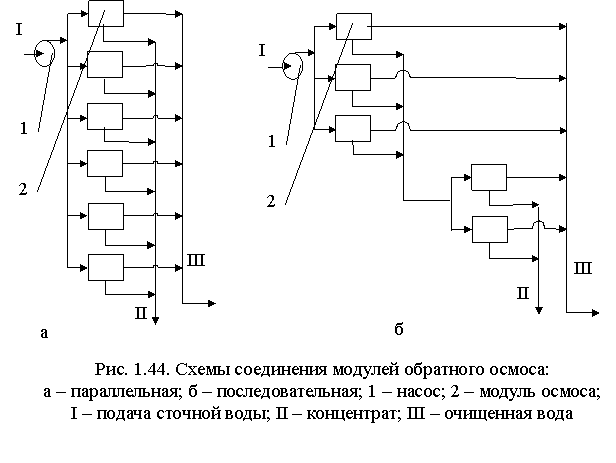
При параллельном соединении (рис. 1.44, а) все модули работают в одинаковых условиях – при одинаковом давлении и коэффициенте выхода фильтрата.
Производительность таких установок низкая. Последовательное соединение (рис. 1.44, б) модулей позволяет увеличить выход фильтрата. Раствор концентрата из первой ступени служит исходной водой для второй ступени. Промежуточного насоса не требуется, т.к.к давление на выходе первой ступени незначительно отличается от давления на входе во вторую ступень (потери напора составляют 0,2-0,3 МПа). Такая схема для двух - и трехступенчатых установок обеспечивает коэффициент выхода фильтрата 70-90 %.












