Олигоэфиры, модифицированные растительными маслами и их жирными кислотами
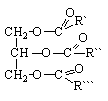
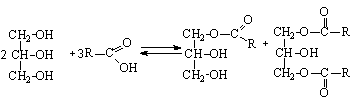
Растительные масла – это смешанные триглицериды карбоновых кислот.
R`, R``, R``` - алифатические радикалы с прямой цепью ненасыщенных и насыщенных жирных кислот общей формулы CnH2n-xCOOH, в которых n = 15-17; x = 0; 2; 4; 6.
К таким маслам относятся в первую очередь тунговое, льняное, подсолнечное, хлопковое, дегидратированное касторовое. Жирные кислоты растительных масел используют и в свободном виде.
Синтез алкидов с использованием в качестве модификаторов растительных масел проводят глицеридным методом, а алкидов, модифицированных их жирными кислотами, – жирнокислотным методом.
По глицеридному методу синтез проводят в две стадии. Первая стадия – алкоголиз растительных масел (переэтерификация); в результате образуются неполные эфиры полиатомных спиртов:
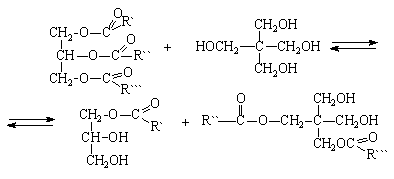
Реакцию переэтерификации проводят в присутствии таких катализаторов, как РbO, CaO, Na2CO3, при 210-240°С. На второй стадии неполные эфиры взаимодействуют с фталевым ангидридом с образованием неполных кислых эфиров.
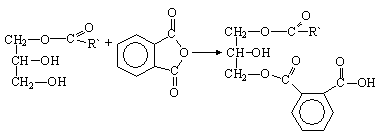
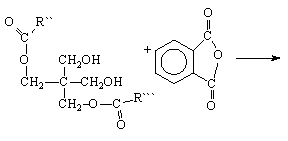 неполный кислый эфир (I)
неполный кислый эфир (I)

неполный кислый эфир (II)
Последние подвергаются поликонденсации:
n (I) + n(II)
![]()

Иногда оказывается целесообразным стадии получения неполного кислого эфира и полиэтерификации разделять во времени и выполнять как отдельные операции, например, в полунепрерывном и непрерывном способах получения алкидов.
Жирнокислотный метод используется для получения алкидов, модифицированных свободными жирными кислотами растительных масел, которые получают предварительным расщеплением последних. Процесс ведут в одну или две стадии. При двухстадийном способе на первой стадии при 150-200°С проводят реакцию между полиатомным спиртом и монокарбоновыми кислотами, в результате которой получают неполные эфиры полиатомных спиртов:
А на второй стадии при 180-210°С проводят реакцию неполных эфиров с фталевым ангидридом, в результате которой образуются алкидные олигомеры разветвленного строения. Процесс на этой стадии идет по той же схеме, что и в случае глицеридного метода.
При одностадийном способе все компоненты загружают одновременно и процесс ведут при постепенном подъеме температуры от 150 до 210°С.
Для контролирования процесса синтеза алкидов используются различные методы. Так, процессы этерификации и полиэтерификации контролируются по изменению концентрации свободных карбоксильных групп в реакционной массе, которая оценивается кислотным числом. Для контроля реакции алкоголиза растительных масел, при которой концентрация функциональных групп не изменяется, используют растворимость неполных эфиров полиатомных спиртов в этаноле. Иногда эту реакцию контролируют по электропроводности.
При получении алкидов, содержащих непредельные жирные кислоты, процесс может осложняться полимеризацией по двойным связям жирнокислотных остатков, приводящей к дополнительному увеличению молекулярной массы и вязкости продукта. Поэтому процесс контролируют и по вязкости реакционной массы.
Органорастворимые алкиды представляют собой разветвленные олигоэфиры с функциональными гидроксильными и карбоксильными группами, которые при модификации маслами или их свободными жирными кислотами содержат также и двойные связи. Их кислотные числа имеют величину от 15 до 30, а гидроксильные числа – от 100-120 мг КОН/г.
Отверждение алкидов в покрытиях может происходить как за счет дальнейшей поликонденсации разветвленных олигоэфиров, так и вследствие окислительной полимеризации радикалов ненасыщенных жирных кислот-модификаторов. Вклад того или иного механизма определяется химическим составом исходных продуктов, а также условиями отверждения олигоэфиров.
Окислительная полимеризация относительно легко протекает уже при комнатной температуре и может быть в еще большей степени ускорена при добавлении сиккативов. Для отверждения за счет поликонденсации необходимы высокие температуры (>150°С). Способность олигоэфира к высыханию в условиях комнатной температуры определяется содержанием двойных связей в их молекулах, что необходимо иметь в виду при составлении рецептур алкидов. Хорошо отверждаются алкиды (олигомеры), молекулы которых содержат не менее 6-7 двойных связей. Это означает, что если для модификации олигоэфира использовать высыхающее масло (например, льняное), то в молекулу достаточно ввести 2-3 жирнокислотных остатка. При модификации полувысыхающими маслами (подсолнечным, хлопковым) необходимо ввести не менее 6 жирнокислотных остатков.
Способность к «высыханию» в условиях комнатной температуры является преимуществом алкидов, модифицированных растительными маслами. Вместе с тем при введении непредельных жирных кислот в макромолекулу алкидов ухудшается светостойкость за счет процессов окислительной деструкции.
Получают также невысыхающие алкиды, модифицированные касторовым маслом. Их обычно называют резилами. Резилы не применяются в качестве пленкообразующих, а служат обычно пластификаторами хлорсодержащих полиолефинов, карбамидоформальдегидных олигоэфиров, эфиров целлюлозы.
Модифицированные маслами (или их кислотами) алкидные олигомеры могут быть органорастворимыми и водоразбавляемыми. Органорастворимые алкидные олигомеры используют обычно в виде растворов в органических растворителях (ксилол, уайт-спирит); водоразбавляемые в водно-органических растворах (обычно в смесях целлозольвов или изопропанола с водой). Наиболее широкое применение в настоящее время находят органорастворимые алкидные олигомеры.
Алкидные полимеры, синтезированные из терефталевой и изофталевой кислот, характеризуются большей теплостойкостью, чем соответствующие полимеры ортофталевой кислоты.
Покрытия из алкидных полимеров, содержащих пиромеллитовую кислоту, обладают большей твердостью и быстрее высыхают, чем покрытия фталевой или изофталевой кислот. Алкидные полимеры на основе хлорэндинового ангидрида имеют пониженную горючесть.
На основе ангидрида бензбициклодикарбоновой кислоты получены алкидные полимеры с повышенной адгезией к подложкам различной природы, повышенной водо - и солестойкости.
На основе хлорангидридов терефталевой и изофталевой кислот, бисфенолов и многоатомных спиртов, содержащих в молекуле более двух гидроксильных групп (глицерин, триметилолпропан, триметилолэтан, флороглюцин), получены полиэфиры повышенной теплостойкости. Технологические процессы и аппаратурное оформление различных алкидных полимеров, получаемых равновесной поликонденсацией, практически аналогичны, но различаются природой исходных мономеров, наличием или отсутствием растворителя, а следовательно, и режимами.
Ниже приведены физико-механические показатели алкидных полимеров общего назначения:
Разрушающее напряжение, МПа
при сжатии 112-140
при растяжении 21-28
при изгибе 490-700
Ударная вязкость, кДж/м2 1,6-1,9
Удельное объемное электрическое сопротивление, Ом×м 1012
Тангенс угла диэлектрических потерь при 60 Гц 0,050-0,060
Диэлектрическая проницаемость при 60 Гц 6,0-6,5
Водопоглощение за 24 ч, % 0,08-0,10
Максимальная температура эксплуатации, °С 176
При производстве алкидных олигомеров по периодической схеме (рис. 38) синтез проводят в реакторе 11 с высокотемпературным обогревом (в данном случае - с электроиндукционным), в который на первой стадии (алкоголиза) загружают масло и полиатомные спирты.
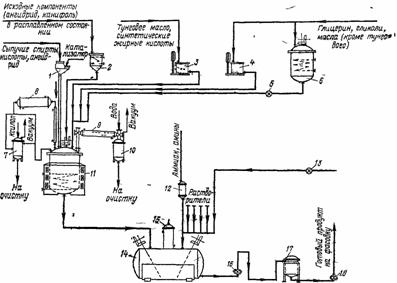
Рис. 38. Технологическая схема производства алкидных олигомеров периодическим методом:
1 - автоматические порционные весы; 2, 3 - обогреваемые весовые мерники; 4 - весовой мерник; 5, 13 – жидкостные счетчики; 6 – аппарат для предварительного подогрева исходных жидких веществ; 7 – разделительный сосуд; 8, 15 – конденсаторы; 9 – сублимационная труба; 10 – мокрый уловитель погонов; 11 – реактор с индукционным обогревом; 12 – объемный мерник; 14 – смеситель;
16, 18 – шестеренчатые насосы; 17 – фильтр
Алкоголиз ведут при 240-260°С в присутствии катализатора (Na2CO3, РbО и др.) в токе инертного газа, контролируя процесс по растворимости продукта в спирте. На этой стадии процесса к реактору 11 подключены сублимационная труба 9 и мокрый уловитель погонов 10. По окончании алкоголиза температуру понижают до 180°С и в реактор вводят расплавленный фталевый ангидрид. Полиэтерификацию проводят при 210-240°С в зависимости от способа получения (блочный или азеотропный), причем в последнем случае в аппарат вводят 2-3% ксилола и соединяют аппарат с конденсатором 8 и разделительным сосудом 7, в котором собирается отогнанная смесь воды и ксилола и происходит ее расслаивание: нижний слой (вода) отводитсяиз разделительного сосуда через нижний штуцер, а ксилол возвращается в реактор 11. Растворение олигоэфира в смеси уайт-спирита и ксилола (до содержания сухого остатка 53 ± 2%) проводят в обогреваемом горизонтальном смесителе 14, в который он подается самотеком из реактора (после предварительного охлаждения до 180°С) под слой предварительно налитого растворителя. Готовый лак очищают на фильтре 17 и отправляют на фасовку.
При производстве алкидов по полунепрерывной схеме операции алкоголиза и получения неполного кислого эфира осуществляют в непрерывном режиме, а стадию полиэтерификации - в периодическом (рис. 39).
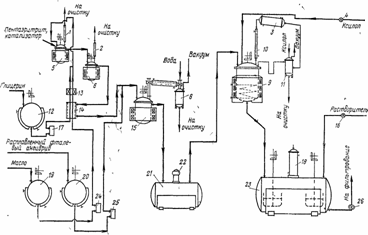
Рис. 39.Технологическая схема производства алкидных олигомеров полунепрерывным методом:
1, 2, 10 - теплообменники; 3, 18 - конденсаторы; 4, 16 - жидкостные счетчики; 5, 6. 9, 15 - реакторы с индукционным обогревом; 7 - сублимационная труба; 8 - мокрый уловитель погонов; 11 - разделительный сосуд; 12, 19-21 - обогреваемые емкости-хранилища; 13 - электрообогреватель; 14 - теплообменник; 17, 24, 25 - насосы-дозаторы; 22 - погружной насос; 23 - смеситель; 26 - шестеренчатый насос
Бесперебойная работа аппаратуры, включенной в эту схему, обеспечивается соответствующим подбором емкостей реакторов и установкой промежуточного хранилища между непрерывной и периодической частями схемы. Алкоголиз проводят в каскаде реакторов 5 и 6 небольшой емкости (2,5 м3), синтез неполного кислого эфира - в реакторе 15, емкостью 3,2 м3. Большой реактор 9 (емкостью 32 м3) предназначен для полиэтерификации азеотропным способом, а горизонтальный смеситель 23 (емкостью 63-80 м3) - для растворения алкида.
Возможная непрерывная схема производства алкидов в колонных аппаратах представлена на рис. 40.
Исходные компоненты, необходимые для алкоголиза масла (пентаэритрит, глицерин, масло и катализатор) смешивают при нагревании в аппарате, откуда реакционная масса подается с помощью дозировочного насоса 7 в секционную колонну с переливными трубками 5, где и проводят алкоголиз при 240-250°С.
Синтез неполных кислых эфиров ведут при 180°С в реакторе 15, куда поступают алкоголизат (из колонны 5) и расплавленный фталевый ангидрид из емкости-хранилища 14. Полиэтерификацию проводят в роторно-дисковой колонне 6 азеотропным способом (температура 200-210°С). Использование роторно-дисковой колонны позволяет проводить процесс в пленочном режиме, что обеспечивает наиболее полное его завершение. Растворение олигоэфира проводят в смесителе 19.
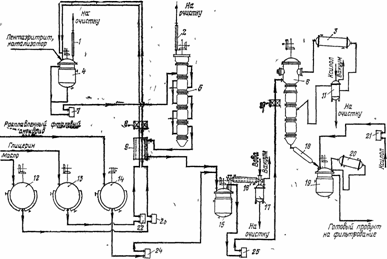
Рис. 40. Технологическая схема производства алкидных олигомеров непрерывным методом:
1, 2, 18 – теплообменники; 3, 20 – конденсаторы; 4, 15 – реакторы, обогреваемые ВОТ; 5 – секционная колонна с переливными трубами; 6 – роторно-дисковая колонна; 7, 21-25 – дозировочные насосы; 8, 10 – электрообогреватели; 9 – теплообменник; 11 – разделительный сосуд; 12-14 – обогреваемые емкости-хранилища; 16 – сублимационная труба; 17 – мокрый уловитель погонов; 19 – смеситель












