Основные закономерности процесса синтеза меламиноформальдегидных олигомеров
Поликонденсация меламина с формальдегидом состоит из серии последовательно-параллельных реакций: гидроксиметилирования меламина и последующей конденсации его метилольных производных.
Гидроксиметилирование меламина происходит по аминогруппам.
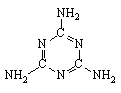 Меламин - амид циануровой кислоты (1,3,5-триамино-2,4,6-триазин);
Меламин - амид циануровой кислоты (1,3,5-триамино-2,4,6-триазин);
Тпл = 351°С
Присутствие трех реакционных центров в молекуле меламина обеспечивает присоединение к нему до шести молекул формальдегида с образованием гексаметилолмеламина:
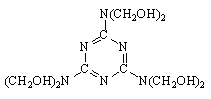
Схема последовательно-параллельных реакций гидроксиметилирования меламина включает образование продуктов с различной степенью замещения. Все реакции в схеме равновесные и протекают с небольшим экзотермическим эффектом (-DН = 13 кДж/моль формальдегида):


Константы равновесия реакций гидроксиметилирования меламина (t = 48°С; рН = 9):
Км,1 = 26,5 К2,3 = 4,4 К3,4 = 2,9 К4,5 = 1,3
К1,2 = 12,0 К2,3¢ = 1,8 К3¢,4¢ = 0,47 К4¢,5 = 21,0
К1,2¢ = 0,85 К2¢,3¢ = 24,5 К3¢,4 = 7,2 К5,6 = 0,6
Уменьшение констант равновесия в ряду Км,1; К1,2; К2,3; К4,5; К5,6 (соответственно 26,5; 12,0; 4,4; 2,9; 1,3 и 0,6) свидетельствует о затруднении гидроксиметилирования с увеличением степени замещения.
В результате гидроксиметилирования обычно образуется смесь продуктов с различным числом метилольных групп в молекуле. Состав смеси в значительной степени зависит от исходного соотношения формальдегида и меламина в реакционной системе.
При соотношении формальдегид/меламин равном 1 в реакционной массе остается значительное количество непрореагировавшего меламина (» 60%). При соотношении, равном 3, основные продукты – моно - и диметилольные производные меламина. При увеличении указанного соотношения исходных веществ до 5-7 в составе продуктов наряду с моно - и диметилольными производными появляется значительное количество три - и тетраметилольных производных. Гексаметилолмеламин обнаруживается в составе продуктов лишь при соотношении формальдегид/меламин > 10, но доля его остается невысокой; даже при увеличении этого соотношения до 30 гексаметилолмеламина образуется лишь около 12%.
Причиной значительного содержания в составе продуктов производных с невысокой степенью метилолирования являются низкие значения констант равновесия реакций гидроксиметилирования. Поэтому, чтобы получить продукты с достаточно большим числом метилольных групп в молекуле, необходим значительный избыток формальдегида. За счет значительного избытка формальдегида удается получать продукты реакции, не содержащие непрореагировавший меламин. Меламин полностью вступает в реакцию лишь при соотношении формальдегид/меламин ³ 7.
Гидроксиметилирование меламина с заметной скоростью протекает даже в отсутствие катализатора, при температурах 35-50°С. Реакция подвержена катализу кислотами и основаниями.
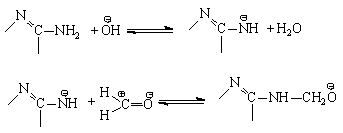
Основной катализ сводится к повышению нуклеофильности меламина за счет отрыва протона от одной из NH2-групп:
Трудность отрыва протона от такого сильного основания, каким является меламин, обуславливает эффективность основного катализа лишь при высоких значениях рН (³ 9).
Специфика меламина, как сильного одноосновного основания, особенно сильно проявляется при кислотном катализе. В присутствии кислоты меламин практически полностью превращается в одноосновную сопряженную кислоту:
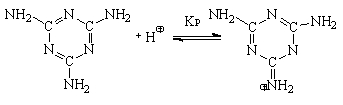
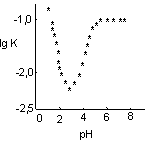
Константа равновесия этой реакции Кр » 105. Поэтому добавление кислоты в количестве до 1 моль на 1 моль меламина (рН в области ³ 2) не только не приводит к увеличению скорости реакции, а, наоборот, замедляет ее из-за низкой активности протонированной формы меламина (рис. 49).
(![]() )
)
Рис. 49. Зависимость логарифма константы скорости реакции гидроксиметилирования (lg k) меламина от рН при катализе НСl. Концентрация формальдегида и меламина равна 0,094 моль/л (при рН = 2,2 соотношение концентраций катализатора НСl и меламина составляет 1)
Поэтому кислотный катализ эффективен лишь при условии, что соотношение кислота:меламин > 1 (рН < 2). В этом случае возможно активирование формальдегида по механизму кислотного катализа с последующим взаимодействием с меламином:
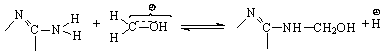
Поэтому скорость реакции гидроксиметилирования при рН < 2 резко возрастает.
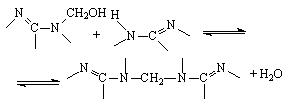
При конденсации метилольных производных меламина происходит образование олигомерных продуктов за счет следующих реакций:
(1)
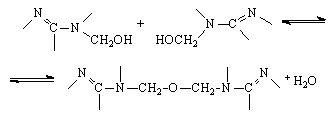
(2)
Реакция (1) преобладает в тех случаях, когда в составе продуктов гидроксиметилирования присутствуют в основном метилольные производные с небольшой степенью замещения. Реакция (2) оказывается преобладающей при условии наличия метилольных производных с более высокой степенью замещения (три-, тетра - и пентаметилолмеламина).
Хотя процесс конденсации метилольных производных меламина, так же как и метилольных производных карбамида, подвержен кислотному катализу, он имеет свои особенности. Так, при уменьшении рН с 7 до 2 скорость конденсации проходит через максимум при рН = 4-4,5. Этот максимум соответствует отношению кислоты-катализатора к метилольному производному меламина, равному 0,5.
Данная особенность обусловлена высокой основностью метилольных производных меламина (рКа диметилольного производного равно 4,5, триметилольного – 3,9). Такая высокая основность приводит к образованию сопряженных кислот, структура которых для ди - и триметилольных производных может быть представлена следующим образом:
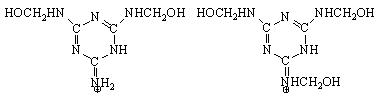
и
Поэтому конденсация метилольных производных в кислой среде может идти за счет взаимодействия нейтральных молекул, сопряженных кислот, а также сопряженных кислот с нейтральными молекулами с образованием метиленовых связей.












