Поликонденсация фенола с формальдегидом при кислотном катализе (новолаки)
Кислотному катализу подвержены все основные реакции, идущие при поликонденсации фенола с формальдегидом. Это – гидроксиметилирование и конденсация, протекающая с участием метилольных производных.
Сущность кислотного катализа гидроксиметилирования – повышение электрофильности формальдегида за счет его протонирования:
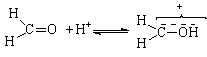
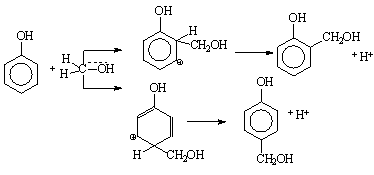
(2)
В кислой среде о - и п-метилольные производные нестабильны и образуют сравнительно устойчивые и долгоживущие ионы карбония, которые, в свою очередь, реагируют как электрофильные агенты с фенолом или с метилольными производными.
Возможная схема реакции о-метилольных производных показана ниже:
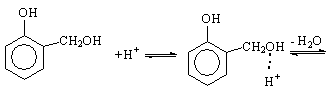
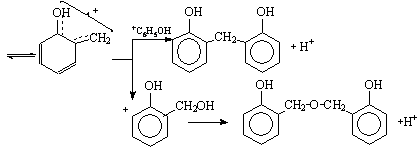
(3)
Аналогичным образом может быть представлено образование о-, п-дигидроксибензилового эфира и о-, п-дигидроксидифенилметана. Образовавшиеся по реакциям (2) и (3) двухатомные фенолы вступают в аналогичные превращения, в результате которых получаются олигомерные продукты.
Кислотный катализ эффективен в области рН 1-4. В более кислых средах проводить процесс нецелесообразно, поскольку в этих условиях снижается активность фенольного компонента в результате его протонирования по гидроксильной группе.
Все рассмотренные реакции протекают легко при довольно низких температурах и сопровождаются значительным выделением тепла (88 кДж/моль фенола, вступившего в реакцию).
При конденсации фенола с формальдегидом в кислой среде по достижении определенной степени конверсии (50-70% по формальдегиду) происходит расслоение реакционной массы. И далее процесс протекает в гетерогенной системе. После расслоения системы мономеры и продукты реакции не распределяются между фазами. Концентрация фенола больше в органической фазе, а формальдегида – в водной.
Структура продуктов конденсации фенола с формальдегидом определяется соотношением исходных веществ. При избытке формальдегида (мольное соотношение СН2О/фенол > 1) нельзя получить плавкие растворимые продукты. Высокая функциональность фенола (f = 3) и нестабильность метилольных производных в кислой среде приводит к образованию полимера с неограниченно развитой пространственной структурой. Поэтому процесс синтеза фенолоформальдегидных олигомеров в кислой среде можно проводить лишь при недостатке формальдегида (т. е. при мольном соотношении СН2О/фенол < 1). В этом случае получают термопластичные фенолформальдегидные олигомеры, не содержащие в своей структуре метилольных групп. Их обычно называют новолачными.
Структура новолачного олигомера представляется следующим образом:
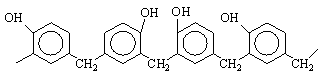
Изомерный состав новолачных олигомеров (соотношение о,о-, о,п - и п-,п-структурных фрагментов) определяется соотношением скоростей реакций, протекающих по орто - и пара-положениям фенольных ядер. Следует иметь в виду, что реакционная способность пара-положения несколько выше, чем орто-положения. Это различие особенно значительно в случае реакции конденсации с участием метилольных производных, но с повышением температуры и рН среды оно уменьшается.
Молекулярная масса новолачных олигомеров определяется соотношением мономеров в исходной смеси, составляя 600-700 (среднечисловая ММ). Отношение
![]()
для этих олигомеров 2,0-2,4, что близко к наиболее вероятному распределению по Флори.
Отсутствие в структуре новолачного олигомера диметиленэфирных мостиков обусловлено низкой долей реакции из-за избытка фенола и склонностью дигидроксибензилового эфира к гидролизу и деструкции с выделением формальдегида в кислых средах.












