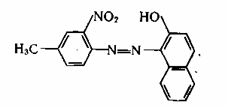
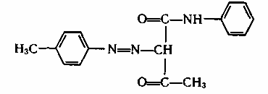
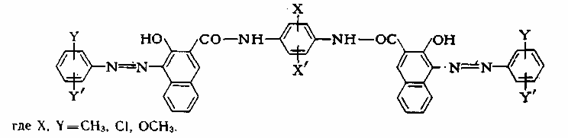
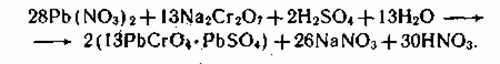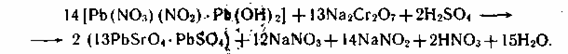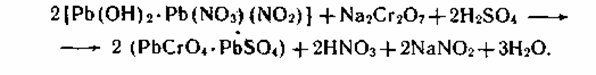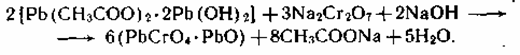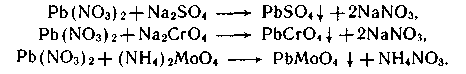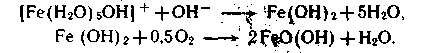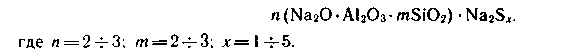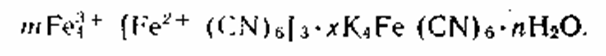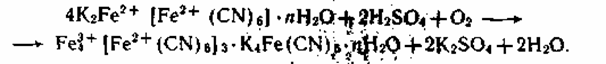Желтые, оранжевые, красные и коричневые неорганические пигменты представлены, главным образом, двумя большими группами химических соединений-хроматами металлов и оксидами железа с разной степенью гидратированности.
Крона.
Нерастворимые или плохо растворимые в воде соли, в кристаллической решетке которых содержатся ионы CrO42 - обусловливающие их цвет, получили чрезвычайное распространение в качестве неорганических пигментов. В зависимости от катиона, входящего в состав соединения, различают свинцовые, цинковые, стронциевые, бариевые и другие крона. Наиболее широкое распространение в промышленности получили свинцовые и цинковые крона.
Цвет всех хроматов, определяющийся широкой полосой поглощения хромат-иона в коротковолновой области видимой части спектра и меняется от лимонно-желтого до красного. На цвет хроматов оказывает влияние катион, входящий в их состав, и кристаллическая структура. Это дает возможность получать крона с чрезвычайно разнообразными оттенками. Независимо от метода получения и используемого сырья, хром в состав кронов входит только в виде хромат-иона, поскольку произведение растворимости хроматов металлов меньше, чем соответствующих бихроматов. Тем не менее, в водном растворе имеет место равновесие, зависящее от рН:
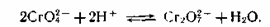
Свинцовые и цинковые крона — токсичные продукты. Особую опасность представляет наличие пыли в производственных помещениях. Тщательной очистки требуют и сточные воды, содержание Cr6+ в которых не должно превышать 0,1 мг/л. Основным способом очистки сточных вод от хромат-ионов является восстановление Cr6+ до Cr3+ с последующим осаждением хрома в виде гидроксида.
Свинцовые крона
Свинцовыми кронами называют хроматы или сульфохроматы свинца общего состава PbCrO4*nPbSO4 или оксихромат состава PbCrO4-PbO.
Хромат свинца, входящий в состав свинцовых кронов, обладает полиморфизмом и может кристаллизоваться в трех кристаллических модификациях — ромбической, имеющей лимонный цвет, моноклинной — желтого цвета, и тетрагональной — красного цвета. Значительное отличие по цвету тетрагональной модификации от ромбической и моноклинной объясняется тем, что две последние модификации относятся к низшей категории симметрии, а тетрагональная — к средней и для нее характерен батохромный сдвиг поглощения в видимой области спектра.
Ромбическая модификация хромата свинца метастабильна. Для ее стабилизации хромат свинца соосаждают с сульфатом. Изоструктурные сульфат и хромат свинца, проявляя изоморфизм, образуют смешанные кристаллы. Сульфат свинца, как и его хромат, полиморфен. Он кристаллизуется в моноклинной и ромбической модификациях, причем ромбическая модификация стабильна. При содержании сульфата свинца 20% (масс.) и более крон кристаллизуется (при соблюдении соответствующих условий) в стабильной ромбической модификации лимонного цвета. В соответствии с этим для лимонных кронов п= 0,2-1,0, для желтых — п= 0-0,1.
Недостатком свинцовых кронов является способность их изменять цвет под действием света, причем уменьшение коэффициента отражения происходит сначала в диапазоне длин волн 640— 700 hm, затем преобладает его уменьшение в диапазоне длин волн 520—640 hm, затем вновь преобладают изменения в длинноволновой области. Эти изменения оптических свойств объясняются протеканием ряда процессов. Прежде всего, это окислительно-восстановительный процесс, в результате которого в поверхностных слоях кристаллической решетки происходит накопление ионов Cr3+ и Pb4 + . Этот процесс сопровождается батохромным эффектом, так как, если цвет хромата обусловлен переходом с переносом заряда, т. е. переходом электрона с лиганда на ион металла в ионе CrO4+, то появление ионов Cr3+ имеющих неспаренные 3d3 электроны, дает возможность осуществления d-d -переходов вследствие расщепления основного состояния на три уровня.

Степень изменения цвета кронов зависит от применяемого пленкообразующего вещества и увеличивается с ростом способности последнего к окислению. Наибольшее изменение цвета кронов при облучении наблюдается в среде алкидных и масляных пленкообразователей.
Для повышения светостойкости рекомендуется модифицировать свинцовые крона соединениями алюминия, титана, кремния, бария, олова, стронция, сурьмы, марганца, висмута, гафния, тория, ниобия, тантала, внедряя их в кристаллическую решетку или осаждая на поверхности в виде гидроксидов. Соединения кремния рекомендуется наносить на поверхность пигмента в виде аморфного оксида. Это, наряду с повышением светостойкости, увеличивает термическую и химическую стойкость пигмента.
Основные физико-технические свойства свинцовых кронов:
Плотность – 6000 кг/м3, Удельная поверхность – 9,4 – 15 м2/г, рН водной вытяжки 5,0‑8,5, Маслоемкость – 6‑25 г/100г, укрывистость 40‑60 г/м2, термостойкость 150‑300 0С.
Желтые и лимонные свинцовые крона используются для получения эмалей, грунтовок и красок как холодного, так и горячего отвержде-ния. Они применяются также для производства полиграфических красок, окрашивания пластмасс и кожи. Оранжевый свинцовый крон используется главным образом для получения противокоррозионных грунтовок и эмалей.
Основной метод получения свинцовых кронов — осаждение пигментов из водных растворов или водных суспензий реакционноспособных соединений. Свинецсодержащими исходными растворами служат растворы нитрата, основного нитрата, основного нитрат-нитрита, ацетата и основных ацетатов свинца различной основности. Можно использовать также суспензии высокоосновного ацетата, хлороксида и высокодисперсного оксида свинца(II). Осаждение производится растворами бихромата или хромата натрия. Для получения сульфохроматов свинца в состав раствора вводят также серную кислоту или сульфат натрия.
Свинцовые крона получают также диспергированием оксида свинца (II) в воде с последующим введением в эту суспензию хромового ангидрида, азотной кислоты и сульфата натрия или серной кислоты. Известен и электрохимический способ получения с использованием в качестве осадителя хромового ангидрида и серной кислоты, а в качестве источника ионов свинца — растворяющегося свинцового анода.
Процессы получения свинцовых кронов, чаще всего применяемые в промышленности, описываются следующими суммарными реакциями:
1. Получение желтого свинцового крона из среднего нитрата свинца:
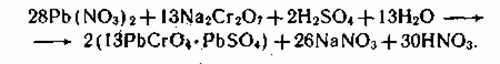
Выделяющаяся азотная кислота связывается вводимым в состав реакционной среды карбонатом кальция. Условия: рН = 5,5-6,0, температура 20—30 0C, избыток соли свинца.
2. Получение желтого свинцового крона из основного нитрат-нитрита свинца:
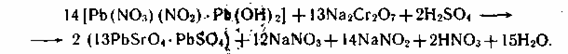
Температура 60—70 0C, рН = 5,5-6,0, избыток соли свинца.
3. Получение желтого свинцового крона из оксида свинца(II) и хромового ангидрида:
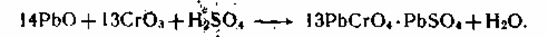
Для активации оксида свинца добавляется небольшое количество азотной кислоты.
4. Получение лимонного крона из среднего нитрата свинца:
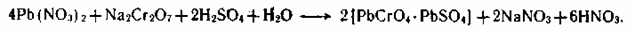
5. Получение лимонного крона из основного нитрат-нитрита свинца:
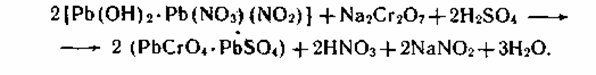
6. Получение оранжевого крона из двухосновного ацетата свинца:
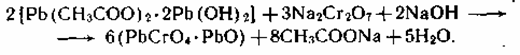
Независимо от основности используемого ацетата, получение оранжевого свинцового крона, являющегося оксихроматом свинца, кристаллизующимся в тетрагональной модификации, возможно лишь при рН³9. Процесс осаждения проводят при температуре 80—90 0C.
Свинцово-молибдатный крон
Свинцово-молибдатный крон по химическому составу является изоморфной смесью хромата, сульфата и молибдата свинца. Красный или оранжевый цвет свинцово-молибдатного крона обусловлен наличием в его составе хромата свинца в тетрагональной кристаллической модификации. Чаще всего получают красный свинцово-молибдатный крон состава
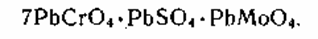
Основные физико-технические свойства свинцово-молибдатного крона: плотность – 5500 кг/м3, удельная поверхность – 12,4 м2/г, рН водной вытяжки 6,6‑7,5, маслоемкость – 20‑23 г/100г, укрывистость 20 г/м2
Свинцово-молибдатный крон является сейчас практически единственным неорганическим пигментом, обладающим чистым красным цветом, и широко применяется для получения различных эмалей, типографских красок и для окрашивания пластмасс. Свинцово-молибдатный крон получают совместным осаждением хромата, сульфата и молибдата свинца:
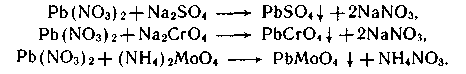
Соосаждение с сульфатом используется для исключения образования в процессе синтеза устойчивой моноклинной модификации. Соосаждение с молибдатом необходимо для осуществления полиморфного превращения первоначального образующейся метастабильной ромбической модификации лимонного цвета в красную тетрагональную.
Цинковые крона
Цинковые крона содержат калий и по составу соответствуют формуле: 4ZnO-xCrO3-0,2xK2O-3H2O, где х= 4 ‑ 2,5. Цинковые крона, применяемые для противокоррозионных грунтовок по черным и цветным металлам, представляют собой основные хроматы цинка. Наиболее применимы трехосновный и четырехосновный хроматы цинка.
Цинковые крона получают главным образом обработкой предварительно диспергированного в воде оксида цинка раствором бихромата калия, подкисленного серной или соляной кислотой. Получают цинковые крона также обработкой оксида цинка растворами хромового ангидрида или смесью хромового ангидрида и бихромата калия.
В настоящее время наибольшее значение имеют грунтовочные цинковые крона (триокси- и тетраоксихроматы цинка). Их свойства будут рассмотрены ниже.
Хромат цинка и калия состава 4ZnO-4CrO3-K2O-3H2O имеет следующие физико-технические свойства:
| Плотность, кг/м3 |
3500 |
| Насыпной объем, м3/кг |
1,6-10-3 |
| рН водной вытяжки |
6,5 |
| Маслоемкость, г/ 100 г |
20—30 |
| Укрывистость, г/м2 |
110 ‑ 120 |
Хроматы цинка и калия применяются для изготовления эмалей и художественных красок.
Цинковые крона нельзя применять для получения водоразбавляемых лакокрасочных материалов из-за заметной растворимости в воде и высокой реакционной способности.